
Der Weg zur personalisierten Hepatitis-D-Behandlung
Hepatitis D ist die bei weitem schwerste Form der chronischen Virushepatitis, die häufig zu Leberversagen, hepatozellulärem Karzinom und zum Tod führt. Das Wissen über die Pathophysiologie der Krankheit und die Wechselwirkungen zwischen Wirt und Virus ist jedoch sehr begrenzt, was die große interindividuelle Variabilität im Verlauf von Hepatitis D erklärt. Das D-SOLVE-Konsortium ("Understanding the individual host response against Hepatitis D Virus to develop a personalized approach for the management of hepatitis D"), das an der MHH/CiiM koordiniert wird, zielt auf ein unabhängiges Screening einer großen multizentrischen Kohorte gut definierter HDV-infizierter Patienten ab, um die individuellen Faktoren, die den Ausgang der Infektion bestimmen, besser zu verstehen und Personen zu identifizieren, die von den derzeit verfügbaren Behandlungen profitieren. In einer sehr kompetitiven Ausschreibung hat das D-SOLVE-Konsortium eine vierjährige Finanzierung in Höhe von 6,75 Millionen Euro aus dem Horizon 2020 EU Horizon Call "Personalisierte Medizin und Infektionskrankheiten: Verständnis der individuellen Wirtsantwort auf Viren (z.B. SARS-CoV-2)" der Europäischen Union erhalten.
Weitere Informationen finden Sie auf der Website des Projekts D-SOLVE.
Hintergrund

Hepatitis D ist die bei weitem schwerste Form der chronischen Virushepatitis, die häufig zu Leberversagen, hepatozellulärem Karzinom und Tod führt. Hepatitis D wird durch eine Koinfektion mit dem Hepatitis-B-Virus (HBV) und dem Hepatitis-D-Virus (HDV) verursacht. Weltweit sind bis zu 20 Millionen Menschen mit dem HDV infiziert, darunter etwa 250 000 Patient:innen in der Europäischen Union. Hepatitis D stellt in bestimmten Regionen Zentralasiens und Afrikas eine große gesundheitliche Belastung dar, ist aber auch in einigen europäischen Ländern wie Rumänien ein besonderes Problem. In den west- und mitteleuropäischen Ländern gibt es eine hohe HDV-Prävalenz in der zugewanderten Bevölkerung, so dass eine angemessene Versorgung eine Herausforderung darstellt.
Das Wissen über die Pathophysiologie der Krankheit und die Wechselwirkungen zwischen Wirt und Virus ist immer noch sehr begrenzt, wobei letzteres der Grund für die große interindividuelle Variabilität im Verlauf der HDV-Infektion ist. Da Hepatitis D in den westlichen Ländern eine seltene Krankheit ist, gibt es bisher keine großen multizentrischen Kohorten von HDV-infizierten Patient:innen mit geeigneten Biobanken. Es gibt auch kein robustes und zuverlässiges Tiermodell, an dem sich die unterschiedlichen Reaktionen des Wirts untersuchen lassen. Bis vor kurzem gab es keine zugelassene antivirale Behandlungsmöglichkeit für Hepatitis D. Pegyliertes Interferon alfa wurde fast zwei Jahrzehnte lang mit sehr begrenztem Erfolg als Off-Label-Therapie eingesetzt. Der Eintrittsinhibitor Bulevirtid erhielt im August 2020 die bedingte EMA-Zulassung und ist nun in einigen europäischen Ländern erhältlich, aber es bleiben noch zahlreiche Fragen zur optimalen Behandlung offen. So ist beispielsweise nicht definiert, welche Patient:innen vorrangig behandelt werden sollen, wie lange die Behandlung dauern soll und was mit Patient:innen mit suboptimalem Ansprechen geschehen soll. Auch die extrem hohen Kosten für dieses Arzneimittel für seltene Leiden stellen in verschiedenen Bereichen ein großes Hindernis dar.
Es besteht daher ein dringender klinischer, sozialer und wirtschaftlicher Bedarf, die individuellen Faktoren, die den Ausgang der Infektion bestimmen, besser zu verstehen und diejenigen Personen zu identifizieren, die von den derzeit verfügbaren Behandlungsansätzen profitieren werden. Das D-SOLVE-Konsortium ist der festen Überzeugung, dass es sich bei Hepatitis D um eine prototypische Infektionskrankheit handelt, die von einem neuartigen individualisierten infektionsmedizinischen Ansatz, der auf einem besseren Verständnis der Immunantwort des Wirtes gegen HDV und der Identifizierung eindeutiger Immun-Biomarker beruht, enorm profitieren könnte.
Das D-SOLVE-Konsortium stellt die Hypothese auf, dass ein umfassendes und unvoreingenommenes Screening einer großen multizentrischen Kohorte gut definierter HDV-infizierter Patient:innen, gefolgt von mechanistischen Studien zur Bestimmung der funktionellen Rolle bestimmter Moleküle, spezifische Parameter und Instrumente identifizieren wird, die einen unmittelbaren Einfluss auf die Behandlung von Patient:innen mit dieser schwersten viralen Lebererkrankung haben können. Überwachungsstrategien für Patient:innen und antivirale Behandlungsansätze könnten personalisiert werden, was die klinische und soziale Krankheitslast verringern, die Lebensqualität verbessern und die durch HDV-Infektionen verursachten direkten und indirekten Kosten senken dürfte.
Ziel
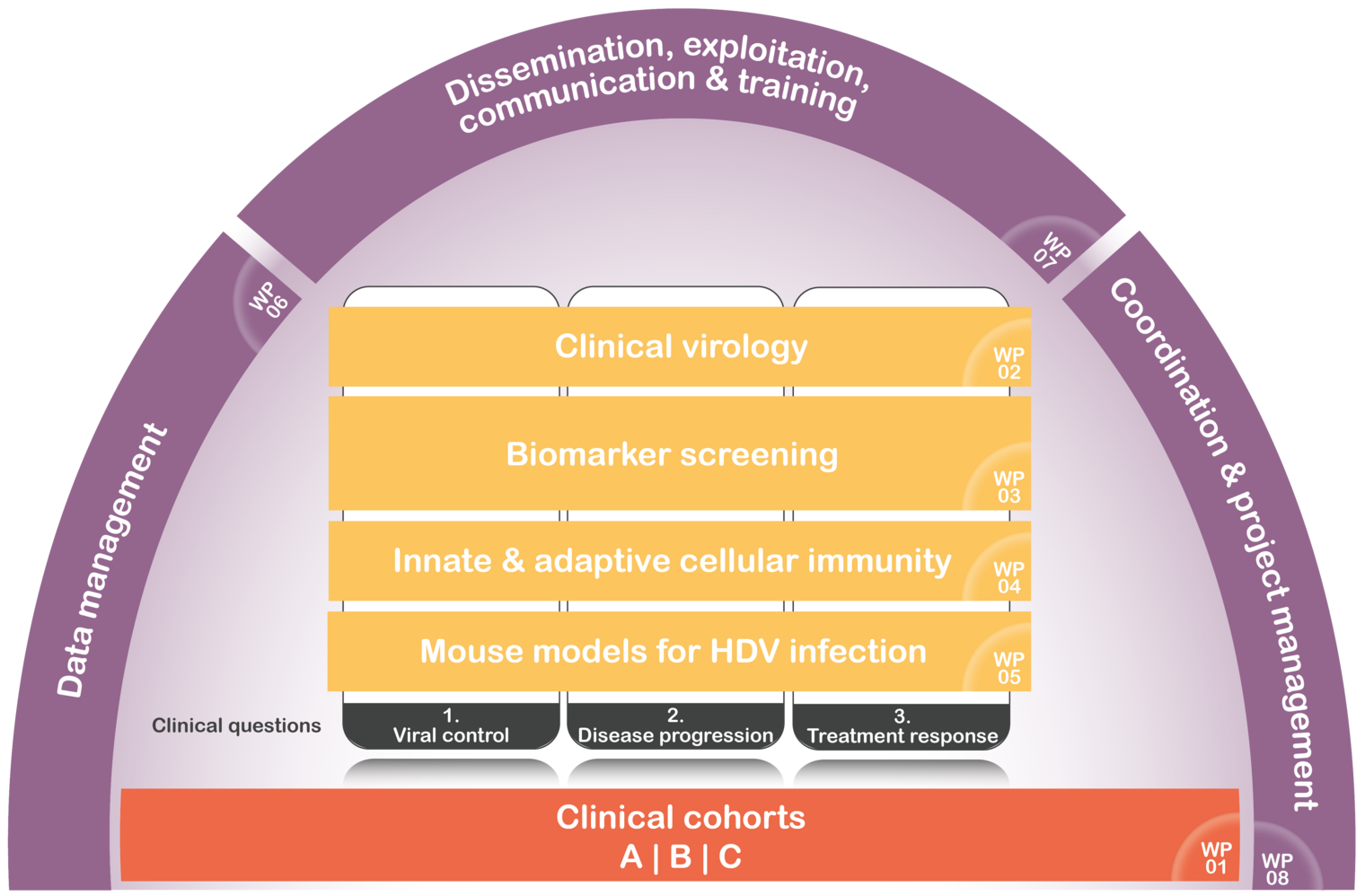
Die drei wichtigsten klinischen Fragen bei der Behandlung von Hepatitis D, die von D-SOLVE behandelt werden sollen, sind folgende
- Virale Kontrolle: Es ist völlig unbekannt, warum einige Patient:innen in der Lage sind, eine HDV-Infektion mit sehr niedrigen HDV-Replikationsraten oder sogar nicht nachweisbarer HDV-RNA zu kontrollieren, während andere eine sehr hohe HDV-Virämie mit HDV-RNA-Werten von über 10 Millionen IU/ml aufweisen. Der Prozentsatz der HDV-RNA-Negativität bei Anti-HDV-positiven Patient:innen liegt zwischen 20 und 50 %. Die einzelnen Faktoren, die mit der Virenkontrolle in Verbindung stehen, sind weitgehend unklar. Die Bestimmung von Biomarkern, die das individuelle Risiko eines viralen Ausbruchs oder Rückfalls anzeigen, ist ein dringender medizinischer Bedarf für die tägliche Behandlung von Hepatitis-D-Patient:innen.
- Fortschreiten der Krankheit: Die chronische Virushepatitis führt zu einer Entzündung mit anschließender Entwicklung einer Leberfibrose, die zu einer Leberzirrhose führen kann. Bei allen Virushepatitis-Infektionen hat sich jedoch gezeigt, dass das Fortschreiten der Fibrose mehrere Jahre und manchmal sogar Jahrzehnte dauern kann. Auch hier sind die Faktoren, die zwischen einem gutartigen und einem aggressiven Krankheitsverlauf unterscheiden, weitgehend unbekannt, insbesondere in den frühen Stadien der Infektion. Ein tieferes Verständnis der Mechanismen, die die unterschiedlichen Ergebnisse erklären und vorhersagen, wäre für das klinische Management von Hepatitis-D-Patient:innen äußerst wünschenswert. Optimale Überwachungsintervalle und Überwachungsinstrumente sind nicht definiert und könnten auf neuen Biomarkern basieren. Darüber hinaus könnte die Entscheidung über die Einleitung potenziell nebenwirkungsanfälliger und kostspieliger antiviraler Behandlungsansätze auf der Grundlage eindeutiger individueller Risikoprofile für langfristige Komplikationen der Lebererkrankung individualisiert werden.
- Ansprechen auf die antivirale Behandlung: Pegyliertes Interferon alfa (PEG-IFNa) wird seit fast zwei Jahrzehnten (off-label) zur Behandlung von HDV-Infektionen eingesetzt. Die Behandlung mit PEG-IFNa ist jedoch mit häufigen und manchmal schweren Nebenwirkungen verbunden und kann bei Patient:innen mit HDV-assoziierter Autoimmunhepatitis zu schweren Hepatitisschüben führen, einem besonders häufigen und manchmal schwerwiegenden Merkmal der HDV-Infektion. Darüber hinaus gibt es keine zuverlässigen Faktoren, die das Ansprechen auf die PEG-IFNa-Behandlung vorhersagen. Es besteht daher ein dringender Bedarf an einer personalisierten Risikostratifizierung, welche Patient:innen eine realistische Chance haben, von einer PEG-IFNa-Therapie zu profitieren. Im Sommer 2020 erteilte die EMA eine bedingte Zulassung für die Behandlung von Hepatitis D für Bulevirtid, einen neuartigen HBV/HDV-Eintrittsinhibitor, der auf den Gallensäuretransporter NTCP abzielt, basierend auf vielversprechenden Ergebnissen aus zulassungsrelevanten Phase-2-Studien. Bulevirtid, ein Peptid, das täglich s.c. injiziert werden muss, führt bei der Mehrheit der Patient:innen zu einem Rückgang der HDV-RNA-Spiegel und einer Verbesserung der biochemischen Krankheitsaktivität, ohne größere systemische Nebenwirkungen zu verursachen. Allerdings sind mehrere Schlüsselfragen zum Einsatz von Bulevirtid noch völlig unklar. So ist z. B. die optimale Behandlungsdauer nach Beginn der Behandlung mit dem Eintrittsinhibitor noch nicht festgelegt. Während einige Patient:innen möglicherweise eine lebenslange Erhaltungstherapie benötigen, gibt es Hinweise darauf, dass viele Patient:innen nach Absetzen des Medikaments eine Immunkontrolle erreichen können. Es besteht jedoch die Sorge, dass schwere Rückfälle zu einem potenziell lebensbedrohlichen Ausbruch der Hepatitis führen können, wenn die Behandlung zu früh beendet wird. Daher werden Biomarker benötigt, um Faktoren zu bestimmen, die eine langfristige Kontrolle von HDV nach Absetzen von Bulevirtid vorhersagen.
D-SOLVE wird diese drei zentralen klinischen Fragen in vier translationalen Forschungspaketen behandeln. Wir werden virologische Merkmale der HDV-Infektion untersuchen, ein breites und unvoreingenommenes Biomarker-Screening durchführen, unterschiedliche angeborene und adaptive Immunreaktionen im peripheren Blut und in der Leber von HDV-infizierten Patient:innen untersuchen und die Auswirkungen identifizierter Moleküle in Mausmodellen erforschen - was auch zu neuen antiviralen Strategien führen könnte.
Arbeitsplan
Für ein so anspruchsvolles Projekt wie das vorliegende haben wir einen Arbeitsplan über einen Zeitraum von 48 Monaten erstellt. Dies gewährleistet eine maximale Erfolgswahrscheinlichkeit, beseitigt oder mildert die Risiken, die mit einem Projekt dieser Art verbunden sind, und ermöglicht eine kontinuierliche Überwachung und Überprüfung der Fortschritte während des gesamten Projektzyklus.
Interdependenzen zwischen den richtigen Forschungs- und Entwicklungs- Arbeitspaketen (work packages, WP) werden sichergestellt. Zur Erreichung der spezifischen WP-Ziele sind die Aktivitäten des Arbeitsplans in acht Arbeitspakete (WPs) gegliedert, von denen jedes aus einer Reihe zusammenhängender Aufgaben besteht, die gemeinsam die Erreichung der Projektziele gewährleisten. Die Fortschritte gegenüber dem Programm, dem Budget und den erzielten Ergebnissen werden regelmäßig vom Projektlenkungsausschuss (project steering committee, PSC) überwacht. Sollte sich ein Arbeitspaket um mehr als einen Monat gegenüber dem geplanten Zeitplan verspäten, wird der Projektkoordinator das PSC darauf aufmerksam machen, und es wird ein Plan vereinbart und umgesetzt, um die Verzögerung aufzuholen.
Bei der Arbeit an der personalisierten Behandlung von chronischer Hepatitis D bilden große, weltweit einzigartige klinische Kohorten (WP1) die Grundlage dieses Projekts, die in den kommenden WPs (2, 3, 4 und 5) zur Beantwortung der drei wichtigsten klinischen Fragen zu den individuellen Determinanten von i) Fibroseprogression, ii) Kontrolle der HDV-Replikation und iii) Ansprechen auf die Behandlung genutzt werden sollen. Der Projektkoordinator wird die wichtigsten regelmäßigen Berichte verfassen, und die Protokolle der Fortschrittssitzungen werden im Laufe des Programms alle sechs Monate über den Projektfortschritt informieren.
WP1 (Klinische Kohorten) ist das erste Arbeitspaket, das im Monat 1 beginnt und sich über die gesamte Projektlaufzeit von 48 Monaten erstreckt. Dieses Arbeitspaket wird die Grundlage für die Arbeitspakete 2 bis 5 und die Bewertung der spezifischen wissenschaftlichen Fragen zu i) Kontrolle der HDV-Replikation, ii) individuellen Determinanten der Fibroseprogression und iii) Behandlungsansprechen bilden. Es werden drei Unterprojekte eingerichtet, wobei das erste in einem Querschnittsansatz 750 Patient:innen erfasst, die das gesamte Spektrum der HDV-Infektion in Europa widerspiegeln, das zweite aus einer retrospektiv-prospektiven Kohorte von Patient:innen mit Leberbiopsien besteht, die vor 10-20 Jahren entnommen wurden, um die Korrelate des intrahepatischen Immunsystems mit dem Fortschreiten der Krankheit zu untersuchen, und das dritte eine prospektive Studie mit Patient:innen sein wird, die mit dem neuen Eintrittsinhibitor Bulevirtid behandelt werden.
WP2 (Klinische Virologie: Testen auf neuartige virologische Marker; HDV- und HBV-Sequenzierung) beginnt im Monat 1 und dauert bis zum Monat 36. Dieses Arbeitspaket ist wichtig, um eine umfassende virologische Charakterisierung dieser Patient:innen durchzuführen, die mit zwei Viren, HBV und HDV, infiziert sind. Da die lokale Diagnostik, insbesondere für HDV, aber auch für neue HBV-Marker, nicht vollständig standardisiert ist, sind zentrale Tests mit optimierter Methodik erforderlich. Darüber hinaus wird WP2 eine eingehende virale Sequenzierung sowohl von HBV als auch von HDV durchführen, was entscheidend sein wird, um den Immundruck auf das Virus zu bestimmen und die Interaktionen zwischen Wirt und Virus zu untersuchen.
WP3 (Biomarker-Screening) beginnt in Monat 1 mit retrospektiven Proben (Kohorten B und D) und wird dann mit den anderen Kohorten während des gesamten Förderzeitraums bis Monat 48 fortgesetzt. Dieses Arbeitspaket wird das Kernprojekt zur Identifizierung neuartiger Biomarker für die drei wichtigsten klinischen Herausforderungen sein, die in D-SOLVE angegangen werden sollen. Das KI und das HZI/CiiM werden das entsprechende Screening in Zusammenarbeit mit der MHH und dem INSERM durchführen.
WP4 (Angeborene und adaptive Immunität) beginnt im Monat 1 und dauert bis zum Monat 48. Dieses von KI und MHH geleitete Arbeitspaket wird die Mechanismen der in WP3 identifizierten Biomarker erforschen, sich aber auch auf hypothesengesteuerte Fragen konzentrieren, insbesondere auf die Untersuchung der angeborenen und adaptiven Reaktionen des intrahepatischen Immunsystems. Intrahepatische Immunantworten sind bei Hepatitis D selten untersucht worden, so dass völlig neue Daten zu erwarten sind, die wahrscheinlich nur im Rahmen dieses D-SOLVE-Konsortiums generiert werden können, das translationales klinisches und grundlegendes Fachwissen kombiniert und die Logistik für den Zugang zu dem erforderlichen Patient:innenmaterial bereitstellt.
WP5 (Mausmodelle für HDV-Infektionen und HDV-induzierte transkriptomische und epigenetische Veränderungen) beginnt im Monat 1 und dauert bis zum Monat 48. In Anbetracht früherer Beobachtungen bei HCV ist es wahrscheinlich, dass eine HDV-Kontrolltherapie entweder durch Interferon-basierte Therapien oder in Kombination mit neuartigen antiviralen Medikamenten wie Bulevirtid die HDV-induzierten Veränderungen der Hepatozyten-Zellkreisläufe oder der angeborenen und adaptiven Immunantwort nur teilweise beseitigen wird. Diese anhaltenden Störungen der Leberzellkreisläufe können zum Fortschreiten der Lebererkrankung und zum Risiko des hepatozellulären Karzinoms (HCC) nach der Heilung beitragen. Dieses Konzept wird dadurch unterstützt, dass HDV in Zelllinien eine DNA-Hypermethylierung und Histonmodifikation hervorruft, was auf die Existenz eines epigenetischen viralen Fußabdrucks schließen lässt, der für die virale Pathogenese und das HCC-Risiko relevant ist. Um diese Frage zu klären, werden wir (1) die HDV-induzierten transkriptomischen und epigenetischen Veränderungen in Lebergeweben und PBMCs aus Kohorten von WP1 untersuchen und ihren Phänotyp vor und nach einer antiviralen Behandlung untersuchen. Anschließend werden wir (2) diese Veränderungen in gut charakterisierten Tiermodellen für HDV-HBV-Koinfektionen vor und nach der Behandlung mit antiviralen Therapien validieren und charakterisieren. (3) Schließlich werden wir untersuchen, wie sich diese Veränderungen auf das Fortschreiten der Krankheit und das Krebsrisiko nach der Heilung auswirken. Durch das Verständnis dieser zugrundeliegenden Mechanismen wird dieses Arbeitsprogramm die Entwicklung neuer Biomarker für den Behandlungserfolg, das Fortschreiten der Lebererkrankung und das HCC-Risiko nach der Heilung ermöglichen.
Die WP 6 (Datenmanagement), 7 (Verbreitung, Verwertung, geistiges Eigentum, Kommunikation und Ausbildung) und 8 (Koordinierung und Projektmanagement) werden während der gesamten Projektlaufzeit durchgeführt.
Partner:innen
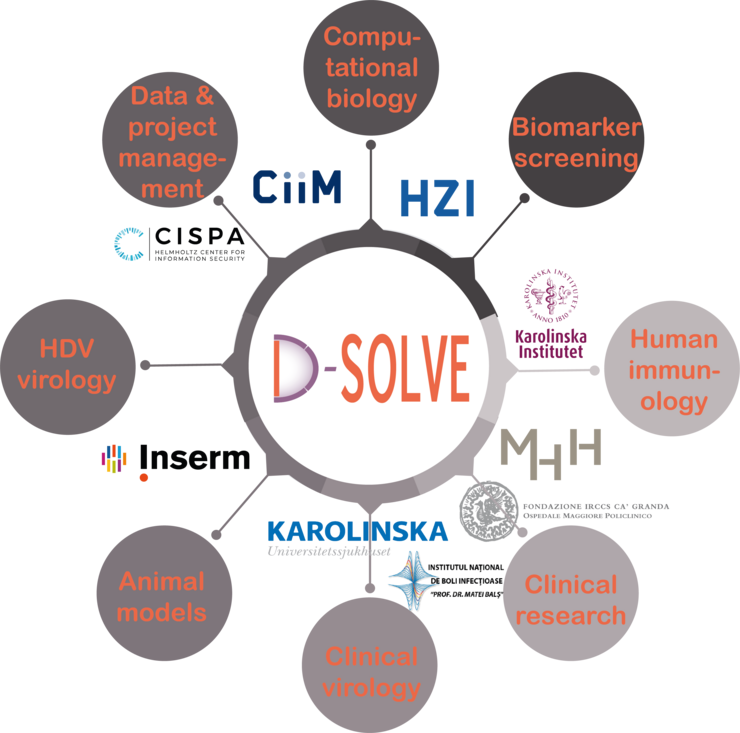
D-SOLVE zielt auf eine individualisierte Behandlung von HDV ab, indem es außergewöhnliche klinische, immunologische, bioinformatische und virologische Fachkenntnisse aus führenden Zentren in Europa vereint. Mehrere der führenden Expert:innen in der europäischen HDV-Forschung tragen zu D-SOLVE bei. Darüber hinaus betreuen klinische Zentren mit herausragender Erfahrung in der translationalen Forschung in Stockholm, Mailand, Hannover und Bukarest einige der größten Einzelkohorten von Patient:innen mit Hepatitis D in Europa. Das Team verfügt über außerordentliches Fachwissen bei der Durchführung eines unabhängigen und breit angelegten Biomarker-Screenings, das von der Wirtsgenetik bis zur Transkriptom- und Proteomanalyse des Wirts reicht, sowie über ein hohes Maß an Expertise in der Bioinformatik. Mechanistische Studien zur Untersuchung verschiedener Moleküle und Signalwege werden von führenden Spezialist:innen auf dem Gebiet der Humanimmunologie, der HDV-Immunität und der Virushepatitis-Forschung unter Verwendung neuer In-vitro- und Tiermodelle durchgeführt. Zudem ermöglicht das CISPA Helmholtz-Zentrum für Informationssicherheit Konzepte für den sicheren Datenaustausch zwischen den Zentren.
Förderung
Das D-SOLVE-Konsortium wird von der Europäischen Union im Rahmenprogramm Horizont Europa (HORIZON) unter der Fördervereinbarung Nr. 101057917 gefördert.

Hepatitis D: B Aware
Das Konsortium D-SOLVE beteiligt sich an der Kampagne „Hepatitis D: B Aware“, die anlässlich des Welthepatitistags, der jedes Jahr am 28. Juli begangen wird, gestartet ist. In kurzen Videos beantworten Forscher:innen wichtige Fragen rund um Hepatitis D. CiiM-Direktor Prof. Markus Cornberg erklärt in seinem Video die Diagnose von Hepatitis D.

Weitere Videos aus der Kampagne finden Sie auf dem Youtube-Kanal von TherVacB
Förderung

Das D-SOLVE-Konsortium wird von der Europäischen Union im Rahmenprogramm Horizont Europa (HORIZON) unter der Fördervereinbarung Nr. 101057917 gefördert.
Weitere Informationen
Projektkoordinator/-Leiter
Prof Heiner Wedemeyer MHH, Germany
Partner:innen
Prof Soo Aleman Karolinska University Hospital, Schweden
Prof Thomas Baumert INSERM, Frankreich
Prof Niklas Björkström Karolinska Institutet, Schweden
Prof Florin Caruntu National Institute for Infectious Diseases "Professor Doctor Matei Balș", Rumänien
Prof Pietro Lampertico Policlinico of Milan, Italien
Prof Yang Li HZI/CiiM, Deutschland
Dr Joachim Lupberger INSERM, Frankreich
Dr Yang Zhang CISPA, Deutschland
MHH/CiiM Mitarbeiter:innen
Prof Markus Cornberg MHH/CiiM, Deutschland
Dr Jennifer Debarry CiiM, Deutschland
Dr Helenie Kefalakes MHH, Deutschland
Dr Lisa Sandmann MHH, Deutschland
Kontakt

